溶液的配制應根據配方各成分的含量分為體積含量[%(體積分數)]或mL/L和質量含量[%(質量分數)]或g/L,在計算用量上有所不同。
1. 體積含量
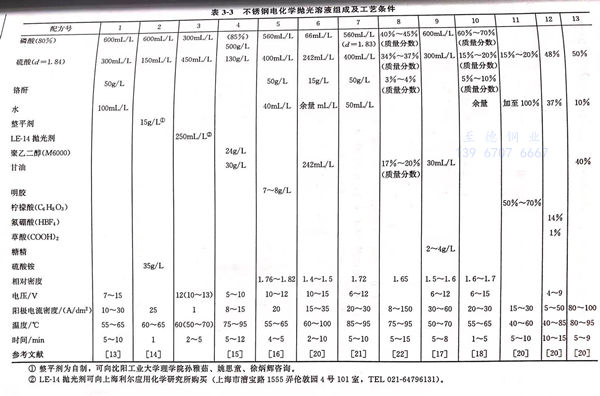
以表3-3中配方5為例,假設槽液容積為1000L,計算用量及配制步驟如下。
①. 磷酸用量
560mL/LX1000L=560L,量取磷酸560L加入槽內。
②. 硫酸用量
400mL/Lx1000=400L,量取硫酸400L,在不斷攪拌下加入磷酸中。
③. 水的用量
40mL/Lx1000L=40L,置于另外一容器中。
④. 鉻酐用量
50g/Lx1000L=50kg,稱取50kg鉻酐加入40L水中,攪拌使溶解成鉻酸溶液。
⑤. 將鉻酸溶液在攪拌下緩慢加入磷酸-硫酸溶液中,攪拌均勻,溶液呈黃色。
⑥. 明膠用量
8g/Lx1000L=8kg.稱取明膠8kg,并粉碎成粉狀,在攪拌下加入⑤步驟的溶液中,加入要緩慢,分少批量撒人,此時起強烈的還原反應,部分Cr6+(即鉻酸中的鉻)轉變為Cr3+,電解液轉變呈黃綠色。
⑦. 在表3-3配方6中不含有明膠而含有甘油,則應將計算量的甘油在攪拌下分批加人槽內,此時也起強烈的還原反應,并產生大量泡沫,為防止泡沫的產生使溶液溢出槽外,加入甘油時要特別小心,溶液也轉呈黃綠色。靜置冷卻。
⑧. 測量溶液的相對密度
用比重計測量冷卻后的槽液,是否在1.76~1.82范圍內,如果超過上限1.82,則應加少量水調整到1.82之內。如果低于1.76,則應將槽液升溫到80℃,蒸除水分,使相對密度上升至1.76以內。
⑨. 通電處理
在陽極上掛上厚度不小于2mm的不銹鋼板,在陰極上掛上鉛板(要有足夠的面積),在溫度70~80℃,DA=60~80A/dm2下通電處理,時間按40A·h/L計算。
⑩. 試投入零件電化學拋光
如果拋光質量良好,即可投入試用。如果拋光質量未達要求,可繼續電解,或分析測量溶液成分含量,進行必要的調整。通電處理的不足可能使溶液中鉻離子、鎳離子含量不足,造成新配電解液拋光表面出現點狀腐蝕,或表面光澤不夠理想。加入鉻酐、甘油、明膠可以使電解液中的六價鉻和三價鉻更快地增加到必需的含量,但鎳離子含量還要靠電解不銹鋼的溶入產生。通電處理可使電解液呈現微綠色,表明已有一定量的鎳離子、鉻離子溶入電解液中,方可獲得試拋光的成功。
2. 質量含量
以表3-3中配方10為例[磷酸60%~70%(質量分數)、硫酸15%~20%(質量分數)、鉻酐5%~10%(質量分數),水余量,相對密度1.6~1.7],配制步驟如下,假設槽體積為1000L.
①. 首先要測量所使用的磷酸和硫酸的相對密度,假定測出的磷酸相對密度d1=1.7,硫酸相對密度d2=1.8。
②. 然后從各種酸的相對密度的化學資料的表中查得:在100g酸液中磷酸含量p1=86.25g,硫酸含量p2=88g。
③. 計算磷酸所需體積V1和硫酸所需體積V2.按以下公式:

⑥. 將鉻酐計算量加入所需水中,攪拌溶解。
⑦. 將磷酸計算量加入鉻酐溶液中,攪拌均勻。
⑧. 將硫酸計算量182.3L在攪拌之下加入步驟⑦的溶液中。
⑨. 測量相對密度
已配好的溶液待溫度冷卻至室溫后用比重計測量相對密度。
如果相對密度高于1.7,應將適量的水加人電解液中,稀釋電解液使相對密度在1.6~1.7范圍內。
如果相對密度在1.6~1.7范圍內,但電解液體積不足,則根據體積不足數,適量按比例補充磷酸、硫酸、鉻酐量。
如果相對密度低于1.6,而體積已足或略超過所配體積,則將電解液加熱至80℃,蒸除水分,直到相對密度達到1.6~1.7的范圍內。
⑩. 通電處理
在陰極上掛上鉛板,在陽極上掛上不銹鋼板,按在本節(1)中所述進行通電處理。在溫度70~80℃下,用DA為60~80A/d㎡,時間按40A.h/L計算通電處理,然后投入試拋光,直到拋光良好為止。



